Rol cardioprotector del Receptor de Estrógenos Acoplado a Proteína G (GPER) en ratas ovariectomizadas: en búsqueda de una alternativa a la Terapia de Reemplazo Hormonal.
CONFORMACIÓN DEL GRUPO:
DIRECCIÓN:
Dra. Verónica De Giusti
INVESTIGADORES:
Dra. Verónica De Giusti
Dr. Ernesto A. Aiello
BECARIO DOCTORAL:
Lic. Alejandro Ibáñez
COLABORADORES:
Dra. María Celeste Villa-Abrille
Lic. Maite Zavala
Dra. Susana Mosca- Dra.
Luisa González Alberaez
Dr. Alejandro Ciocci Pardo
TÉCNICOS:
Med. Vet. Juan Manuel Lofeudo
Mónica Rando
Leandro Di Cianni
Omar Castillo
RESUMEN:
Es ampliamente conocido el rol cardioprotector de los estrógenos durante la etapa fértil de la mujer. Esta protección se pierde con la llegada de la menopausia, en donde los valores plasmáticos de dichas hormonas disminuyen notablemente; y así, las enfermedades cardiovasculares se convierten en la principal causa de mortalidad durante dicha etapa. En un intento por dar solución a la situación se diseñaron las terapias de reemplazo hormonal (TRH), durante las cuales se pensaba que la reintroducción de los estrógenos permitiría prevenir la aparición de eventos cardiovasculares. Al contrario de lo que se pensaba, las TRH no tuvieron los efectos buscados, e incluso tuvieron que ser suspendidas en forma anticipada.
En los últimos años ha surgido un novedoso receptor de estrógenos acoplado a proteína G (GPER), el cual se ubica en las membranas celulares y ejerce efectos no genómicos a través principalmente de la vía de las quinasas PI3K-AKT. Interesantemente, se describió que la mayoría de los efectos cardioprotectores de los estrógenos son llevados a cabo tras la activación del GPER, y no de sus receptores clásicos. Además, se ha sintetizado tanto un agonista (G1) como un antagonista (G15) selectivos para el GPER que ha permitido investigar de forma aislada la participación del receptor en la fisiopatología cardiovascular.
Es así, como surgió la principal pregunta del proyecto, que fue si sería sólo la disminución de los estrógenos la causa de la mayor incidencia de eventos cardiovasculares en la mujer menopáusica, o si habría algo más que lo explicara, y si en ese “algo más” pudiera estar implicada una alteración en la vía de señalización del GPER.
Con esta pregunta inicial, surgieron otras, que estuvieron más destinadas a investigar los cambios celulares que pudiesen explicar lo observado clínicamente en las mujeres menopaúsicas, y más aún que se pudiesen convertir en posibles blancos de acción de una futura terapia.
La tercer pregunta, que se transformó en el principal objetivo de nuestro proyecto es si la terapia crónica con G1 podría prevenir los cambios observados en un modelo de menopausia como las ratas ovariectomizadas (OVX) y transformarse así en una posible terapia alternativa a la TRH.
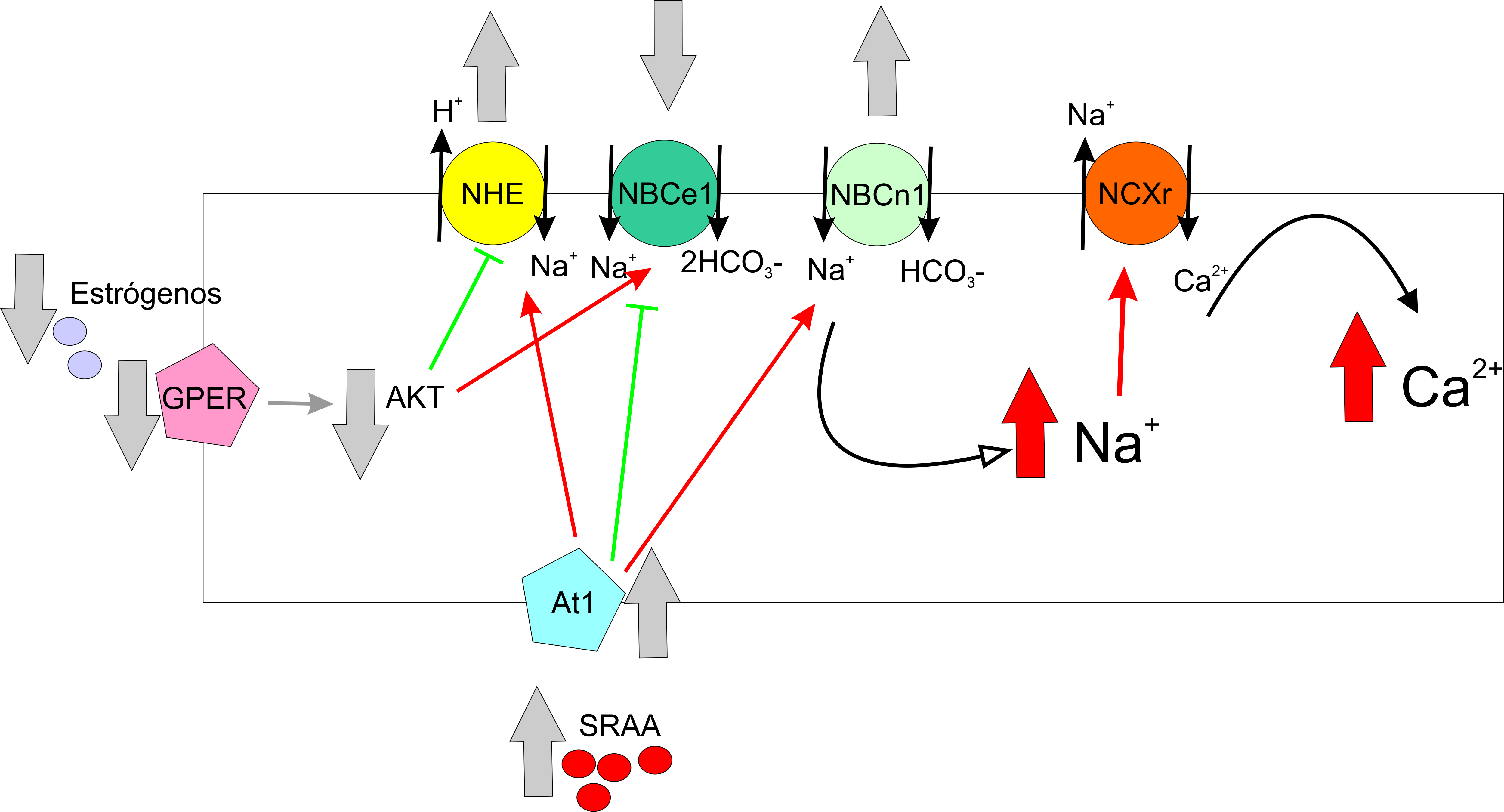
La hipótesis de nuestro proyecto puede resumirse en la figura en donde planteamos que:
En la etapa menopaúsica, al conocido descenso de los niveles estrogénicos, se añade una disminución en la expresión y/o función del GPER y su vía de señalización intracelular; que sumado a una hiperactividad del sistema renina-angiotensina-aldosterona (SRAA) lleva a un remodelado de la expresión y/o función de los transportadores alcalinizantes de las células cardiacas. Esta remodelación incluye un aumento de la actividad del intercambiador sodio/protón (NHE) y de la isoforma electroneutra del cotransportador sodio/bicarbonato (NBCn1), acompañado de una disminución de la isoforma electrogénica del cotransportador (NBCe1). Como es conocido que estas alteraciones están asociadas a un aumento del sodio intracelular, y al consecuente aumento del calcio (por activación del modo reverso del intercambiador sodio/calcio, NCXr), mediador ampliamente conocido de alteraciones cardíacas como eventos arrítmicos, hipertrofia, mayor daño tras isquemia/reperfusión y mayor área de infarto, pensamos que estos cambios podrían explicar al menos en parte, las alteraciones cardiovasculares en la etapa menopaúsica. Por último, pensamos que el tratamiento con G1, al ser capaz de aumentar la expresión y activar selectivamente al GPER, prevendrá estos cambios y representará una posible terapia alternativa a la TRH y una solución a la principal causa de mortalidad en la mujer menopaúsica.